Herpes viruses
Peer reviewed by Dr Colin Tidy, MRCGPLast updated by Dr Toni Hazell, MRCGPLast updated 19 May 2022
Meets Patient’s editorial guidelines
- DownloadDownload
- Share
- Language
- Discussion
- Audio Version
Medical Professionals
Professional Reference articles are designed for health professionals to use. They are written by UK doctors and based on research evidence, UK and European Guidelines. You may find one of our health articles more useful.
In this article:
Continue reading below
Herpesvirus structure
Human herpesvirus
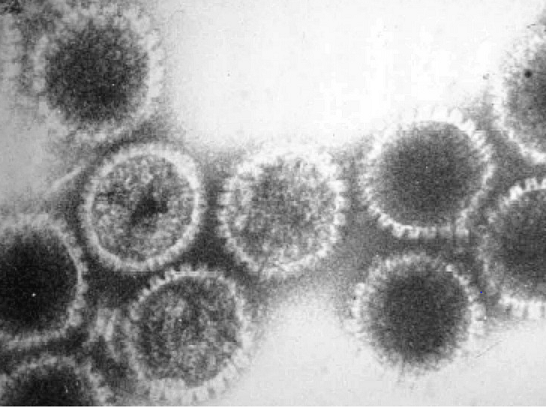
© George W Beran, via Wikimedia Commons
The herpesvirus particle has a very complex structure:
The large double-stranded DNA genome assumes a toroidal shape (like a doughnut), wound round a protein core, further surrounded by a complex icosahedral nucleocapsid, about 100 nm in diameter.
Outside the capsid is the tegument, a protein-filled region appearing amorphous in electron micrographs.
On the outside of the particle is the lipid bilayer envelope, which contains a large number of glycoproteins.
Herpesvirus family types
Back to contentsThere are eight currently identified members of the herpesvirus family. They are ubiquitous and extremely well adapted pathogens. The name comes from the Greek 'herpein' - 'to creep', describing the chronic, latent or recurrent nature of infections.
Herpes simplex type I (HSV-1).
Herpes simplex type II (HSV-2).
Varicella-zoster virus (VZV/HHV-3).
Epstein-Barr virus (EBV/HHV-4).
Cytomegalovirus (CMV/HHV-5).
Herpesvirus type 6 (HBLV/HHV-6).
Herpesvirus type 7 (HHV-7).
Kaposi's sarcoma herpesvirus (KSHV/HHV-8).
They belong to the following three families:
Alpha-herpesviruses: HSV-1 and HSV-2; VZV - these have a relatively short reproductive cycle, variable host range, efficiently destroy infected cells and establish latent infections primarily in sensory ganglia.
Beta-herpesviruses: CMV, HHV-6 and HHV-7 - these have long reproductive cycles and a restricted host range. Infected cells often enlarge. Latency can be maintained in the white cells of the blood, kidneys, secretory glands and other tissues.
Gamma-herpesviruses: EBV and HHV-8 - these are specific for either T or B lymphocytes, and latency is often demonstrated in lymphoid tissue.
Continue reading below
Herpes simplex virus types I and II (HSV-1 and HSV-2)1
Back to contentsSee also the separate Oral Herpes Simplex, Genital Herpes Simplex, Herpes Simplex Eye Infections and Encephalitis and Meningoencephalitis articles.
Primary infection occurs through a break in the mucous membranes of the mouth or throat, via the eye or genitals or directly via minor abrasions in the skin.
Many individuals are infected with HSV-1 by 1-2 years of age; HSV-2 infection tends to be with the onset of sexual activity.
Initial infection is usually asymptomatic, although there may be minor local vesicular lesions. Local multiplication is followed by viraemia and systemic infection and subsequent lifelong latent infection with periodic reactivation.
During primary infection, the virus enters peripheral sensory nerves and migrates along axons to sensory nerve ganglia in the CNS - hence managing to escape the host's immune response.
Between reactivations, the virus is truly latent - viral DNA is maintained as an episome (not integrated) with limited expression of specific virus genes required for the maintenance of latency. The delicate balance of latency may be upset by various disturbances - physical (eg, injury, ultraviolet light, hormones, menstruation) or psychological (eg, stress, emotional upset).
Reactivation of latent virus leads to recurrent disease - virus travels back down sensory nerves to surface of body and replicates, causing tissue damage:
Manifestations of primary HSV infection
Systemic infection: eg, fever, sore throat, and lymphadenopathy. It often passes unnoticed. If immunocompromised, it may be life-threatening with fever, lymphadenopathy, pneumonitis, and hepatitis.
Gingivostomatitis: ulcers filled with yellow slough appear in the mouth.
Herpetic whitlow: a breach in the skin allows the virus to enter the finger, causing a vesicle to form. .
Traumatic herpes (herpes gladiatorum): vesicles develop at any site where HSV is ground into the skin by brute force.
Eczema herpeticum: HSV infection of eczematous skin; usually seen in children.
Herpes simplex meningitis: this is uncommon and usually self-limiting; typically, HSV-2 in women during a primary attack - see the separate Meningitis article.
Genital herpes: usually HSV-2, although either virus can appear in the mouth or the genitals if there has been cross-transmission through orogenital sex. See the separate Genital Herpes Simplex article.
HSV keratitis: manifests with corneal dendritic ulcers. Avoid steroids.
Herpes simplex encephalitis: usually HSV-1. It spreads centripetally - eg, from cranial nerve ganglia, to frontal and temporal lobes. Suspect if the patient has a fever, fits, headaches, odd behaviour, dysphasia, hemiparesis, or coma or subacute brain stem encephalitis, meningitis, or myelitis. See also the separate Encephalitis and Meningoencephalitis article.
Diagnosis
Rising antibody titres in 1° infection.
Viral culture.
PCR for fast diagnosis.
Varicella-zoster virus (VZV/HHV-3)2
Back to contentsThe complete sequence of VZV genome is known, ~125 kilo base pairs (kbp) in length. It infects a variety of human and animal cell types in vitro and gives rise to two distinct clinical syndromes in vivo:
Varicella (chickenpox)
Infection normally occurs in childhood (~90%), entering via the respiratory tract or conjunctiva.
After multiplication at the inoculation sites, the virus spreads to the bloodstream and reticuloendothelial system.
Secondary multiplication involves skin and mucosa, producing vesicles filled with very high titres of infectious virus.
Zoster (shingles)
After primary infection, the virus persists in the sensory ganglia of the CNS.
It is not clear if this is a latent or a persistent infection, but 'reactivation' takes place after many years and leads to infection and tissue damage in the dermatome served by the infected ganglia.
This is most serious when cranial nerves are involved, affecting the face/head. Where the eye is involved, severe sight impairment can result.
See also the separate Chickenpox and Shingles articles.
Continue reading below
Epstein-Barr virus (EBV/HHV-4)
Back to contentsEBV/HHV-4 is widespread in most human populations. It infects human B-lymphocytes (generally non-productive infection) and epithelial cells (productive infection). It is linked with a wide range of diseases, including several different types of tumour.
Disease | Details of EBV involvement3 |
Infectious mononucleosis ('glandular fever') | Primary infection, self-limiting. Occurs in ~50% of primary infections of adolescents and young adults. |
EBV found as latent infection in 97% of endemic, 15-85% of sporadic and 30-40% of AIDS-linked Burkitt's lymphoma cases (common African manifestation). | |
Sporadic lymphoma; latent EBV found in ~50% of cases. | |
B-lymphoproliferative disease | Lymphoproliferative disease/lymphomas, almost exclusively in the immunocompromised host, especially post-transplant (as a result of immunosuppressive drug therapy) and in AIDS. Might occur in primary infection or persistent infection. |
Rare genetic immune dysfunction results in fatal primary infection. | |
Malignant squamous epithelial tumour of the nasopharynx; (common Chinese and Southeast Asian manifestation) cells contain latent virus. | |
Viral replication in the superficial layers of the tongue epithelium results in a benign lesion, almost exclusively in HIV-positive individuals. |
See links in the table for further information. EBV has also been associated with other diseases, including:
EBV-associated gastric carcinoma.4
Several autoimmune diseases, such as systemic lupus erythematosus, rheumatoid arthritis and multiple sclerosis. However, it is not clear whether EBV plays a role in the pathogenesis of these diseases.5
Cytomegalovirus (CMV/HHV-5)
Back to contentsSee the separate Cytomegalovirus article.
Herpesvirus 6 (HBLV/HHV-6)
Back to contentsHHV-6 is associated with roseola infantum (exanthem subitum) or 'sixth disease'.6
A minority of HHV-6 infections in children manifest as roseola, with an abrupt onset of high fever lasting 3-5 days, followed by an erythematous maculopapular rash that appears as temperature subsides.7 The rash is initially on the trunk, then spreads centrifugally to the face and limbs.
The rest of infections either present as acute nonspecific febrile illness or are asymptomatic.
Complications of childhood infection include febrile convulsions and, rarely, encephalitis.8
Antibody titres are highest in children and decline with age.
Herpesvirus 7 (HHV-7)
Back to contentsHHV-7 infects almost all children by the age of three years and persists lifelong, with the shedding of infectious virus in saliva.
It is similar to (HHV-6 in its genetic content and many of its biological properties, including the ability to cause at least some cases of roseola infantum.6
Kaposi's sarcoma-associated herpesvirus (KSHV/HHV-8)
Back to contentsSee also the separate Kaposi's Sarcoma article.
HHV-8 rates vary around the world: high in central Africa, low in the USA and Western Europe with intermediate rates in Mediterranean countries.9 HHV-8 is detectable in Kaposi's sarcoma lesions. HHV-8 may also be associated with:10
Body cavity-based lymphomas (BCBLs) of B-cell origin.
Castleman's disease (a rare, non-neoplastic condition where collections of lymph gland tissue develop throughout the body).
Hyperplastic lymphadenopathy.
Further reading and references
- Sandgren KJ, Bertram K, Cunningham AL; Understanding natural herpes simplex virus immunity to inform next-generation vaccine design. Clin Transl Immunology. 2016 Jul 29;5(7):e94. doi: 10.1038/cti.2016.44. eCollection 2016 Jul.
- Herpesviridiae Taxonomy Browser.
- All the Virology on the WWW
- Gilden D, Mahalingam R, Nagel MA, et al; Review: The neurobiology of varicella zoster virus infection. Neuropathol Appl Neurobiol. 2011 Aug;37(5):441-63. doi: 10.1111/j.1365-2990.2011.01167.x.
- Glandular fever (infectious mononucleosis); NICE CKS, March 2020 (UK access only)
- Iizasa H, Nanbo A, Nishikawa J, et al; Epstein-Barr Virus (EBV)-associated gastric carcinoma. Viruses. 2012 Dec;4(12):3420-39.
- Lossius A, Johansen JN, Torkildsen O, et al; Epstein-Barr virus in systemic lupus erythematosus, rheumatoid arthritis and multiple sclerosis-association and causation. Viruses. 2012 Dec;4(12):3701-30.
- Stone RC, Micali GA, Schwartz RA; Roseola infantum and its causal human herpesviruses. Int J Dermatol. 2014 Apr;53(4):397-403.
- Zerr DM, Meier AS, Selke SS, et al; A population-based study of primary human herpesvirus 6 infection. N Engl J Med. 2005 Feb 24;352(8):768-76.
- Gewurz BE, Marty FM, Baden LR, et al; Human herpesvirus 6 encephalitis. Curr Infect Dis Rep. 2008 Jul;10(4):292-9.
- Schwartz RA, Micali G, Nasca MR, et al; Kaposi sarcoma: a continuing conundrum. J Am Acad Dermatol. 2008 Aug;59(2):179-206; quiz 207-8.
- Wolz MM, Sciallis GF, Pittelkow MR; Human herpesviruses 6, 7, and 8 from a dermatologic perspective. Mayo Clin Proc. 2012 Oct;87(10):1004-14. doi: 10.1016/j.mayocp.2012.04.010. Epub 2012 Jul 21.
Continue reading below
Article history
The information on this page is written and peer reviewed by qualified clinicians.
Next review due: 28 Mar 2027
19 May 2022 | Latest version

Ask, share, connect.
Browse discussions, ask questions, and share experiences across hundreds of health topics.

Feeling unwell?
Assess your symptoms online for free